Грипп — наиболее опасное инфекционное заболевание, передающееся воздушным путем. Для него характерна сезонность и быстрая распространенность. Поражает преимущественно дыхательные пути, способствует появлению интоксикации, лихорадки и часто вызывает осложнения.
Содержание:
Что это такое
Пути передачи и причины
Вирус гриппа А
Симптомы заболевания
Методы лечения
Осложнения
Профилактика
Меры предосторожности при общении с больным
Что это такое
Грипп А относится к респираторно-вирусным инфекциям с преимущественным поражением дыхательной системы. Имеет короткий инкубационный период, быстрое распространение и высокий риск возникновения осложнений.
В процессе заболевания происходит размножение возбудителя на слизистой поверхности эпителиальной ткани глотки, трахеи, носовой полости. В зависимости от локализации вируса, развиваются характерные симптомы в виде сильного кашля, болей в горле, заложенности носа и других признаков.
Отмечается высокая температура тела на фоне скопления продуктов распада пораженных клеток и тканей, остатки которых попадают в кровяное русло. Также возрастает проницаемость сосудов из-за повреждения эндотелия. Поэтому возможно развитие небольшого кровоизлияния в дыхательные органы, и в том числе головной мозг.
Возбудитель гриппа оказывает общее негативное воздействие на иммунную и кровеносную системы. Это может стать причиной вторичных патологий вирусного или инфекционного характера, которые значительно усугубляют течение болезни и приводят к появлению осложнений.
Пути передачи и причины
Причина гриппа — поражение организма вирусными штаммами А типа.
Основными источниками инфекционного процесса выступают люди, больные или носители, также животные и птицы.
Заражение осуществляется воздушным путем, период от проникновения вируса в организм до появления первых признаков составляет не более 2 дней. Поэтому заболевание характеризуется высокой степенью заразности.
Способствующими факторами вирусной инфекции выступает снижение иммунной системы, близкий контакт с больными людьми и наличие сопутствующих патологий.
В группу риска развития гриппа А, входят:
Женщины в период вынашивания ребенка.
Маленькие дети дошкольного возраста.
Сотрудники здравоохранения.
Лица, подверженные частому стрессу, имеющие новообразования, дефицит витаминов, придерживающиеся строгой диеты.
Вирус гриппа А
Вирус гриппа А относится к группе ортомиксовирусов. Он опасен, обладает высокой степенью мутации. Это единственный тип, способный вызывать пандемию и быстрое распространение в обществе.
Наибольшую активность проявляет в осенний и весенний сезон. В качестве потенциальных хозяев возбудителя могут выступать различные животные, птицы, люди. Благодаря этому, вирус быстро приспосабливается и изменяет генетическую информацию за короткий промежуток времени.
За счет наличия в их структуре 2 белков: гемагглютинина и нейраминидазы, врачам удается дифференцировать патологию от других инфекционно-вирусных заболеваний.
Как правило, главной причиной возникновения гриппа А у людей считается не сам возбудитель, а его подтипы h2N1 и H3N2.
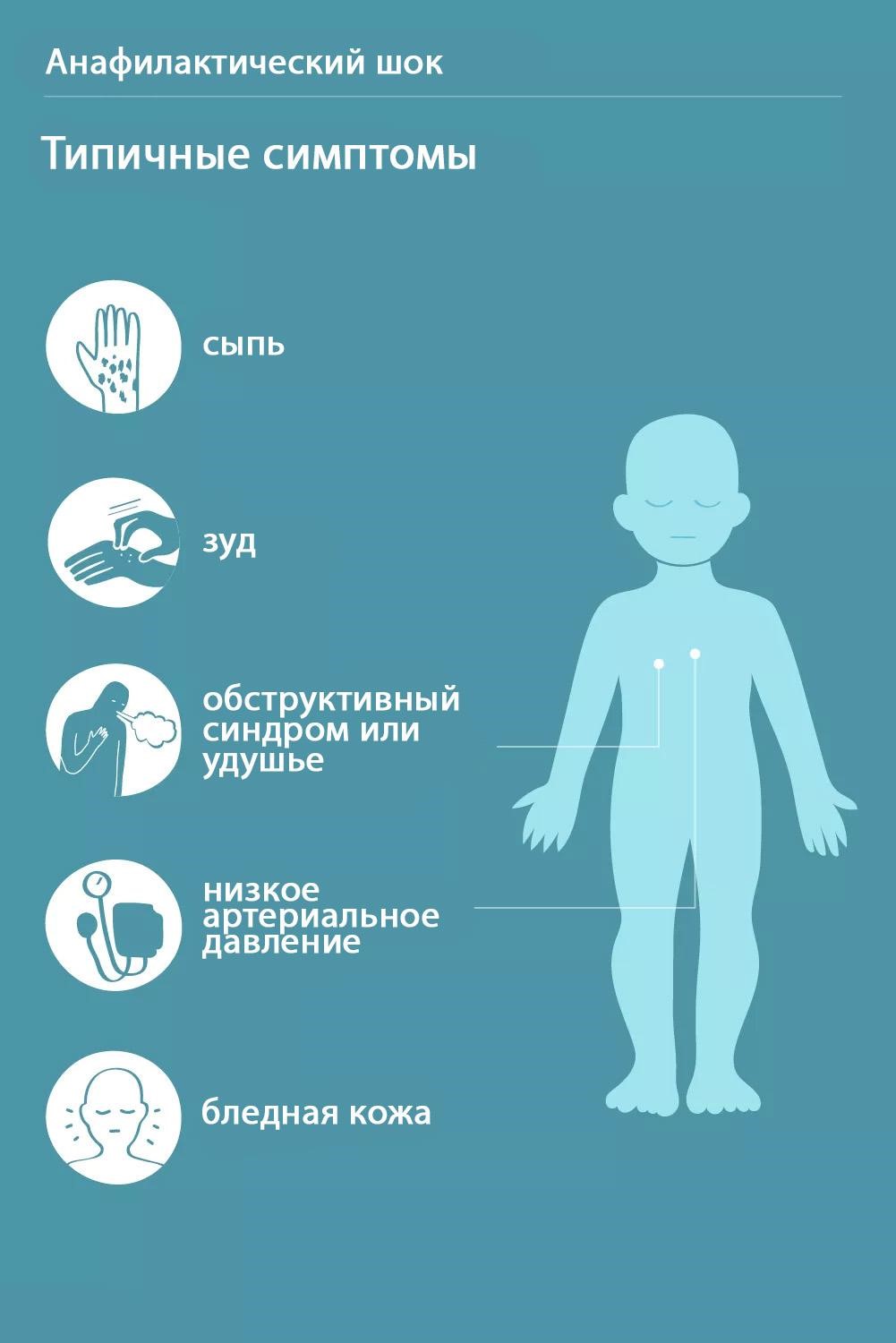
Симптомы заболевания
Первые симптомы патологии возникают через 2 дня после заражения, редко по истечению 4 суток.
На начальных стадиях болезнь сопровождается сильной лихорадкой до 39 С, слабостью, недомоганием, незначительным насморком с сохранением носового дыхания и першением горла.
По мере деятельности возбудителя в организме, отмечаются следующие явные признаки:
Головная боль.
Озноб, чередующийся с жаром.
Болезненные ощущения в горле.
Кашель, чаще сухого характера.
Выраженный насморк, возможна заложенность носа.
Сильная слабость.
Сонливость.
Ломота и боль во всем теле.
Как правило, восстановление температуры наступает через неделю без медицинского вмешательства. При отсутствии осложнений, кашель проходит спустя 7-10 дней.
Если вирусная инфекция протекает в особо тяжелой форме и сопровождается бледностью кожных покровов, развитием цианоза, длительной повышенной температурой тела, болями в грудной области и нарушением деятельности сердечно-сосудистой системы, необходимо вызвать скорую помощь.
Методы лечения
Лечебные мероприятия наступают после подтверждения диагноза на основе клинических данных и осмотра пациента.
Люди, вошедшие в группу риска и имеющие тяжелую форму патологии, должны проходить терапию в стационаре. В остальных случаях, необходимые лечебные процедуры можно осуществить в домашних условиях.
Методы борьбы с гриппом заключаются в следующем:
Ограничение контакта больного человека со здоровыми.
Профилактические меры.
Фармакологическая терапия.
Главной задачей при инфекции является купирование симптомов и причины. Поэтому основными группами лекарственных средств при гриппе А считаются противовирусные, противовоспалительные, жаропонижающие, сосудосуживающие препараты. Дополнительно назначают антигистаминные, противокашлевые средства, гормоны и витамины.
Курс и длительность приема определяет врач на основе состояния больного.
Для большей эффективности лечения важно соблюдать дистанцию с другими людьми, пользоваться индивидуальными вещами, соблюдать постельный режим и необходимое питание. Рацион предпочтительно обогатить клетчаткой, фруктами, овощами и белковыми продуктами. В сутки рекомендуется пить не менее 1, 5 л жидкости.
Осложнения
Грипп может повлечь развитие осложнений. Чаще им подвержены дети и люди со слабым иммунитетом. Они связаны с поражением нервной системы и появлением вторичного инфицирования.
Основными осложнениями выступают воспалительные патологии дыхательных путей, менингит, энцефалит, судорожные припадки, психоз.
Реже наблюдаются перикардит, миокардит, токсический шок.
Профилактика
Профилактические мероприятия инфекционного заболевания включают:
Сбалансированное питание
Укрепление иммунитета.
Соблюдение гигиены.
Отсутствие стресса.
Активный образ жизни.
Своевременное лечение заболеваний.
Вакцинация.
Меры предосторожности при общении с больным
Чтобы исключить заражение гриппом А, важно при контакте с инфицированным держать расстояние, использовать медицинскую маску, укреплять собственный иммунитет.
При проживании на одной территории необходимо часто делать уборку, проветривать квартиру, пользоваться личными вещами, принимать витамины и другие иммунные комплексы.
Опубликовано: 30 Октября 2020
Автор
Все представленные на сайте материалы предназначены исключительно для образовательных целей и не предназначены для медицинских консультаций, диагностики или лечения. Администрация сайта, редакторы и авторы статей не несут ответственности за любые последствия и убытки, которые могут возникнуть при использовании материалов сайта.
Influenza A virus subtype H3N2
Influenza A virus subtype H3N2 (A/H3N2) is a subtype of viruses that causes influenza (flu). H3N2 viruses can infect birds and mammals. In birds, humans, and pigs, the virus has mutated into many strains. In years in which H3N2 is the predominant strain, there are more hospitalizations.[1]
Classification[edit]
H3N2 is a subtype of the viral genus Influenzavirus A, which is an important cause of human influenza. Its name derives from the forms of the two kinds of proteins on the surface of its coat, hemagglutinin (H) and neuraminidase (N). By reassortment, H3N2 exchanges genes for internal proteins with other influenza subtypes.
Seasonal H3N2 flu[edit]
Seasonal influenza kills an estimated 36,000 people in the United es each year. Flu vaccines are based on predicting which «mutants» of h2N1, H3N2, h2N2, and influenza B will proliferate in the next season. Separate vaccines are developed for the Northern and Southern Hemispheres in preparation for their annual epidemics. In the tropics, influenza shows no clear seasonality. In the past ten years, H3N2 has tended to dominate in prevalence over h2N1, h2N2, and influenza B. Measured resistance to the standard antiviral drugs amantadine and rimantadine in H3N2 has increased from 1% in 1994 to 12% in 2003 to 91% in 2005.[2]
Seasonal H3N2 flu is a human flu from H3N2 that is slightly different from one of the previous year’s flu season H3N2 variants. Seasonal influenza viruses flow out of overlapping epidemics in East Asia and Southeast Asia, then trickle around the globe before dying off. Identifying the source of the viruses allows global health officials to better predict which viruses are most likely to cause the most disease over the next year. An analysis of 13,000 samples of influenza A/H3N2 virus that were collected across six continents from 2002 to 2007 by the WHO’s Global Influenza Surveillance Network showed the newly emerging strains of H3N2 appeared in East and Southeast Asian countries six to nine months earlier than anywhere else. The strains generally reached Australia and New Zealand next, followed by North America and Europe. The new variants typically reached South America after an additional six to nine months, the group reported.[3]
Swine flu[edit]
Pigs can harbor influenza viruses adapted to humans and others that are adapted to birds, allowing the viruses to exchange genes and create a pandemic strain.
A 2007 study reported: «In swine, three influenza A virus subtypes (h2N1, H3N2, and h2N2) are circulating throughout the world. In the United es, the classic h2N1 subtype was exclusively prevalent among swine populations before 1998; however, since late August 1998, H3N2 subtypes have been isolated from pigs. Most H3N2 virus isolates are triple reassortants, containing genes from human (HA, NA, and PB1), swine (NS, NP, and M), and avian (PB2 and PA) lineages. Present vaccination strategies for swine influenza virus (SIV) control and prevention in swine farms typically include the use of one of several bivalent SIV vaccines commercially available in the United es. Of the 97 recent H3N2 isolates examined, only 41 had strong serologic cross-reactions with antiserum to three commercial SIV vaccines. Since the protective ability of influenza vaccines depends primarily on the closeness of the match between the vaccine virus and the epidemic virus, the presence of nonreactive H3N2 SIV variants suggests current commercial vaccines might not effectively protect pigs from infection with a majority of H3N2 viruses.»[4]
Avian influenza virus H3N2 is endemic in pigs in China, and has been detected in pigs in Vietnam, contributing to the emergence of new variant strains. Pigs can carry human influenza viruses, which can combine (i.e. exchange homologous genome subunits by genetic reassortment) with H5N1, passing genes and mutating into a form which can pass easily among humans. H3N2 evolved from H2N2 by antigenic shift and caused the Hong Kong Flu pandemic of 1968 and 1969 that killed up to 750,000 humans. The dominant strain of annual flu in humans in January 2006 was H3N2. Measured resistance to the standard antiviral drugs amantadine and rimantadine in H3N2 in humans had increased to 91% by 2005. In August 2004, reers in China found H5N1 in pigs.[5]
Flu spread, by season[edit]
This section needs to be upd. Please up this article to reflect recent events or newly available rmation. (December 2014) |
Hong Kong Flu (1968-1969)[edit]
The influenza viruses that caused Hong Kong flu (magnified 100,000 s)
The Hong Kong Flu was a flu pandemic caused by a strain of H3N2 descended from H2N2 by antigenic shift, in which genes from multiple subtypes reassorted to form a new virus. This pandemic of 1968 and 1969 killed an estimated one million people worldwide.[6][7][8] The pandemic infected an estimated 500,000 Hong Kong residents, 15% of the population, with a low death rate.[9] In the United es, 100,000 people died.[10]
Both the H2N2 and H3N2 pandemic flu strains contained genes from avian influenza viruses. The new subtypes arose in pigs coinfected with avian and human viruses and were soon transferred to humans. Swine were considered the original «interte host» for influenza, because they supported reassortment of divergent subtypes. However, other hosts appear capable of similar coinfection (e.g., many poultry species), and direct transmission of avian viruses to humans is possible. h2N1 may have been transmitted directly from birds to humans (Belshe 2005).[11]
The Hong Kong flu strain d internal genes and the neuraminidase with the 1957 Asian flu (H2N2). Accumulated antibodies to the neuraminidase or internal proteins may have resulted in much fewer casualties than most pandemics. However, cross-immunity within and between subtypes of influenza is poorly understood.
The Hong Kong flu was the first known outbreak of the H3N2 strain, though there is serologic evidence of H3N2 infections in the late 19th century. The first record of the outbreak in Hong Kong appeared on 13 July 1968 in an area with a density of 500 people per acre in an urban setting. The outbreak reached maximum intensity in two weeks, lasting six weeks in total. The virus was isolated in Queen Mary Hospital. Flu symptoms lasted four to five days.[9]
By July 1968, extensive outbreaks were reported in Vietnam and Singapore. By September 1968, it reached India, the Philippines, northern Australia and Europe. That same month, the virus entered California from returning Vietnam War troops. It reached Japan, Africa and South America in 1969.[9]
Fujian flu (2003-2004)[edit]
Fujian flu refers to flu caused by either a Fujian human flu strain of the H3N2 subtype or a Fujian bird flu strain of the H5N1 subtype of the Influenza A virus. These strains are named after Fujian province in China.
A/Fujian (H3N2) human flu (from A/Fujian/411/2002(H3N2)-like flu virus strains) caused an unusually severe 2003-2004 flu season. This was due to a reassortment event that caused a minor clade to provide a haemagglutinin gene that later became part of the dominant strain in the 2002-2003 flu season. A/Fujian (H3N2) was made part of the trivalent influenza vaccine for the 2004-2005 flu season.[12]
2004-2005 flu season[edit]
The 2004-05 trivalent influenza vaccine for the United es contained:
- an A/New Caledonia/20/99 (h2N1)-like virus
- an A/Fujian/411/2002 (H3N2)-like virus
- a B/Shanghai/361/2002-like virus.[12]
2005-2006 flu season[edit]
The vaccines produced for the 2005-2006 season used:
- an A/New Caledonia/20/1999-like(h2N1)
- an A/California/7/2004-like(H3N2) (or the antigenically equivalent strain A/New York/55/2004)
- a B/Jiangsu/10/2003-like viruses
2006-2007 flu season[edit]
The 2006-2007 influenza vaccine composition ed by the World Health Organization on 15 February 2006 and the US FDA’s Vaccines and Biological Products Advisory Committee on 17 February 2006 used:
- an A/New Caledonia/20/99 (h2N1)-like virus
- an A/Wisconsin/67/2005 (H3N2)-like virus (A/Wisconsin/67/2005 and A/Hiroshima/52/2005 strains)
- a B/Malaysia/2506/2004-like virus from B/Malaysia/2506/2004 and B/Ohio/1/2005 strains which are of B/Victoria/2/87 lineage[13]
2007-2008 flu season[edit]
The composition of influenza virus vaccines for use in the 2007-2008 Northern Hemisphere influenza season ed by the World Health Organization on 14 February 2007[14] was:
- an A/Solomon Islands/3/2006 (h2N1)-like virus
- an A/Wisconsin/67/2005 (H3N2)-like virus (A/Wisconsin/67/2005 (H3N2) and A/Hiroshima/52/2005 were used at the )
- a B/Malaysia/2506/2004-like virus[15][16]
«A/H3N2 has become the predominant flu subtype in the United es, and the record over the past 25 years shows that seasons dominated by H3N2 tend to be worse than those dominated by type A/h2N1 or type B.» Many H3N2 viruses making people ill in this 2007-2008 flu season differ from the strains in the vaccine and may not be well covered by the vaccine strains. «The CDC has analyzed 250 viruses this season to determine how well they match up with the vaccine, the report says. Of 65 H3N2 isolates, 53 (81%) were characterized as A/Brisbane/10/2007-like, a variant that has evolved [notably] from the H3N2 strain in the vaccine-A/Wisconsin/67/2005.»[17]
2008-2009 flu season[edit]
The composition of virus vaccines for use in the 2008-2009 Northern Hemisphere influenza season ed by the World Health Organization on February 14, 2008[18] was:
- an A/Brisbane/59/2007 (h2N1)-like virus
- an A/Brisbane/10/2007 (H3N2)-like virus
- a B/Florida/4/2006-like virus (B/Florida/4/2006 and B/Brisbane/3/2007 (a B/Florida/4/2006-like virus) were used at the )[19][20]
As of May 30, 2009: «CDC has antigenically characterized 1,567 seasonal human influenza viruses [947 influenza A (h2), 162 influenza A (H3) and 458 influenza B viruses] collected by U.S. laboratories since October 1, 2008, and 84 novel influenza A (h2N1) viruses. All 947 influenza seasonal A (h2) viruses are to the influenza A (h2N1) component of the 2008-09 influenza vaccine (A/Brisbane/59/2007). All 162 influenza A (H3N2) viruses are to the A (H3N2) vaccine component (A/Brisbane/10/2007). All 84 novel influenza A (h2N1) viruses are to the A/California/07/2009 (h2N1) reference virus selected by WHO as a potential candi for novel influenza A (h2N1) vaccine. Influenza B viruses currently circulating can be divided into two distinct lineages represented by the B/Yamagata/16/88 and B/Victoria/02/87 viruses. Sixty-one influenza B viruses tested belong to the B/Yamagata lineage and are to the vaccine strain (B/Florida/04/2006). The remaining 397 viruses belong to the B/Victoria lineage and are not to the vaccine strain.»[21]
2009-2010 flu season[edit]
The vaccines produced for the 2009-2010 season used:
- an A/Brisbane/59/2007(h2N1)-like virus
- an A/Brisbane/10/2007 (H3N2)-like virus
- a B/Brisbane 60/2008-like antigens[22]
A separate vaccine was available for pandemic h2N1 influenza using the A/California/7/2009-like pandemic h2N1 strain.[23]
2010-2011 flu season[edit]
The vaccines produced for the 2010-2011 season used:
- an A/California/7/2009-like (pandemic h2N1)
- an A/Perth/16/2009-like (H3N2)-like virus
- a B/Brisbane/60/2008-like antigens[23]
2011-2012 flu season[edit]
The vaccines produced for the 2011-2012 season used:
- an A/California/07/2009 (h2N1)-like virus
- an A/Victoria/210/2009 (an A/Perth/16/2009-like strain) (H3N2)-like virus
- a B/Brisbane/60/2008-like virus[24]
2012-2013 flu season[edit]
The vaccines produced for the Northern Hemisphere 2012-2013 season used:
- an A/California/07/2009 (h2N1)-like virus
- an A/Victoria/361/2011 (H3N2)-like virus
- a B/Massachusetts/2/2012-like virus,[25] which replaced B/Wisconsin/1/2010-like virus[26]
In January 2013, influenza activity continued to increase in the United es and most of the country experienced high levels of influenza-like-illness (ILI), according to CDC’s latest FluView report. Reports of influenza-like-illness (ILI) are nearing what have been peak levels during moderately severe seasons, and CDC continues to influenza vaccination and antiviral drug treatment when appropriate at this . On January 9, 2013, the Boston Government declared a public health emergency for H3N2 influenza.[27]
2014-2015 flu season[edit]
The vaccines produced for the Northern Hemisphere 2014-2015 season used:
- A/California/7/2009 (h2N1)pdm09-like virus
- A/Texas/50/2012 (H3N2)-like virus
- B/Massachusetts/2/2012-like virus,[28]
Quadrivalent vaccines include a B/Brisbane/60/2008-like virus.[29] The CDC announced that drift variants of the A (H3N2) virus strain from the 2012-2013 potentially foretold a severe flu season for 2014-2015.[30][31]
2015-2016 flu season[edit]
The vaccines produced for the Northern Hemisphere 2015-2016 season used:
- A/California/7/2009 (h2N1)pdm09-like virus
- A/Switzerland/9715293/2013 (H3N2)-like virus
- B/Phuket/3073/2013-like virus. (This is a B/Yamagata lineage virus)
The «Split Virion» vaccine distributed in 2016 contained the following strains of inactivated virus:
- A/California/7/2009 (h2N1)pdm09 — like strain (A/California/7/2009, NYMC X-179A)
- A/Hong Kong/4801/2014 (H3N2) — like strain (A/Hong Kong/4801/2014, NYMC X-263B)
- B/Brisbane/60/2008 — like strain (B/Brisbane/60/2008, wild type)[32]
2016-2017 flu season[edit]
- A/California/7/2009 (h2N1)pdm09-like virus,
- A/Hong Kong/4801/2014 (H3N2)-like virus
- B/Brisbane/60/2008-like virus (B/Victoria lineage)[33]
Quadrivalent influenza vaccine adds:
- B/Phuket/3073/2013-like strain
2017-2018 flu season[edit]
- A/Michigan/45/2015 (h2N1)pdm09-like virus
- A/Hong Kong/4801/2014 (H3N2)
- B/Brisbane/60/2008-like virus (B/Victoria lineage)[34]
Quadrivalent influenza vaccine adds
- B/Phuket/3073/2013-like[B/Yamagata lineage]
2020-SH(southern hemisphere)[edit]
Quadrivalent-
A/Brisbane/02/2018 (h2N1)pdm09-like virus
A/SouthAustralia/34/2019 (H3N2)-like virus
B/Washington/02/2019-like virus [B/Victoria lineage]
B/Phuket/3073/2013-like virus [B/Yamagata lineage]
See also[edit]
- 2009 swine flu pandemic
- Bird flu
- Dog flu
- Horse flu
- Human flu
- Swine flu
References[edit]
- ^ «Pinkbook | Influenza | Epidemiology of Vaccine Preventable Diseases | CDC». CDC. 2019-03-29. Retrieved 6 June 2019. Greater number of hospitalizations during years that A(H3N2) is predominant
- ^ Ronald Ban This Season’s Flu Virus Is Resistant to 2 Standard Drugs. New York s. January 15, 2006
- ^ CIDRAP d 2009-05-01 at the Wayback Machine article Study: New seasonal flu strains launch from Asia 16 April 2008
- ^ René Gramer, Marie; Hoon Lee, Jee; Ki Choi, Young; Goyal, Sagar M.; Soo Joo, Han (2007). «Serologic and genetic characterization of North American H3N2 swine influenza A viruses». Canadian Journal of Veterinary Re. 71 (3): 201-206. PMC 1899866. PMID 17695595.
- ^ WHO (28 October 2005). «H5N1 avian influenza: line» (PDF). d from the original (PDF) on 27 July 2011.
- ^ Paul, William E. (2008). Fundamental Immunology. p. 1273. ISBN 9780781765190 .
- ^ «World health group issues alert Mexican president tries to isolate those with swine flu». Associated Press. April 25, 2009. Retrieved 2009-04-26.
- ^ Mandel, Michael (April 26, 2009). «No need to panic … yet Ontario officials are worried swine flu could be pandemic, killing thousands». Toronto Sun. Retrieved 2009-04-26.
- ^ a b c Starling, Arthur (2006). Plague, SARS, and the Story of Medicine in Hong Kong. HK University Press. p. 55. ISBN 978-962-209-805-3 .
- ^ «1968 Pandemic (H3N2 Virus)». Centers for Disease Control and Prevention. U.S. Department of Health and Human Services. Retrieved 16 March 2020.
- ^ Chapter Two : Avian Influenza by Timm C. Harder and Ortrud Werner from excellent free on-line book Influenza Report 2006
- ^ a b CDC article Up: Influenza Activity-United es and Worldwide, 2003-04 Season, and Composition of the 2004-05 Influenza Vaccine 2 July 2004
- ^ CDC fluwatch d 2010-03-08 at the Library of Congress Web s B/Victoria/2/87 lineage
- ^ «14 February 2007: WHO rmation meeting (Morning)».
- ^ ed composition of influenza virus vaccines for use in the 2007-2008 northern hemisphere influenza season. WHO
- ^ WHO-ed composition of influenza virus vaccines for use in the 2007-2008 influenza season (PDF)
- ^ CIDRAP article Flu widespread in 44 es, CDC reports 15 February 2008
- ^ «14 February 2008: rmation meeting (Morning)». d from the original on 19 September 2009.
- ^ «WHO website ation for 2008-2009 season».
- ^ WHO-ed composition of influenza virus vaccines for use in the 2008-2009 influenza season d 2008-05-21 at the Wayback Machine (PDF)
- ^ CDC article «2008-2009 Influenza Season Week 21 ending May 30, 2009» May 30, 2009
- ^ «ed composition of influenza virus vaccines for use in the 2009-2010 influenza season».
- ^ a b «Weekly U.S. Influenza Surveillance Report — Seasonal Influenza (Flu) — CDC». 2018-12-07.
- ^ «U S Food and Drug Administration Home Page». 2019-08-27.
- ^ «WHO s new B strain for next season’s flu vaccine». Center for infectious Disease Re and Policy. 21 Feb 2013. Retrieved 2 October 2013.
- ^ «ed composition of influenza virus vaccines for use in the 2013 southern hemisphere influenza season». World Health Organization. 20 Sep 2012. Retrieved 8 December 2012.
- ^ «Mayor declares flu emergency in Boston». Boston Herald. 9 Jan 2013. Retrieved 10 January 2013.
- ^ «What You Should Know for the 2014-2015 Influenza Season». Center for Infectious Disease Re and Policy. Retrieved 30 December 2014.
- ^ «WHO — ed composition of influenza virus vaccines for use in the 2014-2015 northern hemisphere influenza season».
- ^ «CDC Press Releases». January 2016.
- ^ «Dr. Mark Dowell urges flu shots despite mutated h3n2 strain». Wyoming Medical Center. December 8, 2014. Retrieved August 31, 2017.
- ^ «Inactivated Influenza Vaccine (Split Virion) BP — Summary of Product Characteristics (SPC) — (eMC)». d from the original on 2017-01-07. Retrieved 2017-01-06.
- ^ Scutti, Susan (September 14, 2017). «What Australia’s bad flu season means for Europe, North America». CNN. Retrieved 28 September 2017.
- ^ Blanton, Lenee; Wentworth, David E.; Alabi, Noreen; Azziz-Baumgartner, Eduardo; Barnes, John; Brammer, Lynnette; Burns, Erin; Davis, C. Todd; Dugan, Vivien G. (2017). «Up: Influenza Activity — United es and Worldwide, May 21-September 23, 2017». MMWR. Morbidity and Mortality Weekly Report. 66 (39): 1043-1051. doi:10.15585/mmwr.mm6639a3. ISSN 0149-2195. PMC 5720887. PMID 28981486.
Further reading[edit]
- Graphic showing H3N2 mutations, amino acid by amino acid, among 207 isolates completely sequenced by the Influenza Genome Sequencing Project.
- Influenza A (H3N2) Outbreak, Nepal
- Hot topic — Fujian-like strain A influenza
- New Scientist: Bird Flu
External s[edit]
- Influenza Re Database Database of influenza sequences and rmation.
Типирование Influenza virus A (h2N1, H3N2)
[09-171] Типирование Influenza virus A (h2N1, H3N2)
2085 руб.
Типирование Influenza virus A (h2N1, H3N2) — идентификация субтипов вируса гриппа типа А путем качественного выявления в исследуемом материале вирусной нуклеиновой кислоты (РНК).
Синонимы русские
Идентификация субтипов h2N1 и H3N2 вируса гриппа А методом полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР).
Синонимы английские
Influenza virus A RT-PCR subtyping, Influenza virus reverse transcription PCR test.
Метод исследования
Полимеразная цепная реакция в режиме реального времени.
Какой биоматериал можно использовать для исследования?
Мазок из зева (ротоглотки) и носа, мокрота.
Общая информация об исследовании
Вирус гриппа относится к РНКсодержащим вирусам. Род вирусов гриппа включает три типа вирусов: А, В и С. Вирусная частица имеет сферическую форму, в центре которой находится генетический материал вируса — РНК, а в оболочке присутствуют сложные белки — гемагглютинин (Н) и нейраминидаза (N). Для вирусов гриппа типа А характерна постоянная изменчивость этих поверхностных белков: на данный момент известно 15 вариантов гемагглютинина и 9 вариантов нейраминидазы. Их сочетание в определенной комбинации определяет субтип вируса. Вирусы субтипов h2N1 и H3N2 вызывают сезонный грипп человека.
Попадая в организм человека, вирус гриппа проникает в клетки эпителия слизистой оболочки дыхательных путей и размножается в них. Пораженные вирусом клетки дегенерируют, погибают и отторгаются. Таким образом, в отделяемом дыхательных путей (слизь, мокрота и т.п.) присутствуют погибшие эпителиальные клетки вместе с вирусными частицами.
Идентификация субтипа вируса проводится методом полимеразной цепной реакции. Принцип метода основан на обнаружении в материале специфичных фрагментов вирусной РНК, их избирательном синтезе с образованием огромного числа копий, что позволяет их легко детектировать, в том числе визуально. К преимуществам метода ПЦР можно отнести:
прямое определение наличия возбудителя — выявление специфического участка РНК возбудителя дает прямое указание на присутствие вируса;
высокую специфичность — в исследуемом материале идентифицируется уникальный, характерный только для данного вируса фрагмент РНК;
высокую чувствительность — ПЦР позволяет обнаружить возбудитель, даже если его исходная концентрация в исследуемом материале чрезвычайно мала.
Однако стоит отметить, что обнаружение вирусной РНК методом ПЦР не обязательно указывает на обнаружение жизнеспособного вируса или продолжающееся его размножение.
Для чего используется исследование?
- Для идентификации субтипа вируса гриппа.
Когда назначается исследование?
При нетипичных проявлениях заболевания;
при высоком риске осложнений от гриппа (возраст более 65 и менее 2 лет, беременные, а также женщины в период первых двух недель после родов, лица с хроническими заболеваниями легких, сердца, почек, пациенты с иммунодефицитом или гематологическими заболеваниями);
при идентификации возбудителя у пациентов, заболевших вне эпидемиологического сезона.
Что означают результаты?
Референсные значения: не обнаружено.
Положительный результат — если искомый фрагмент вирусной РНК обнаружен — инфицирование вирусом гриппа А определенного субтипа.
Отрицательный результат — если искомый фрагмент вирусной РНК не обнаружен — отсутствие инфекции.
Что может влиять на результат?
Количество дней, прошедшее от начала болезни (после 4 дней возрастает вероятность необнаружения вируса).
Исследуемый образец — при инфекции нижних дыхательных путей вирус может не выявляться в образце, полученном из верхних дыхательных путей (мазки из носа, ротоглотки). В таких случаях необходимо повторить анализ с исследованием отделяемого нижних дыхательных путей.
Важные замечания
- У иммунокомпетентных лиц с неосложненным гриппом вирусовыделение в верхних дыхательных путях, как правило, значительно уменьшается после 4 дней болезни, соответственно, снижается вероятность выделения возбудителя. Поэтому образцы для исследования у таких пациентов должны быть получены в первые четыре дня заболевания, когда выделение вируса максимально. И напротив, у пациентов с ослабленным иммунитетом и при инфекции нижних дыхательных путей (вирусная пневмония) выделение вируса в бронхиальный секрет сохраняется дольше.
- Ожидание результата исследования или отрицательный результат при очевидной клинической картине не должны быть препятствием для назначения противовирусной терапии.
Также рекомендуется
Общий анализ крови с лейкоцитарной формулой
С-реактивный белок
Influenza virus A/h2, РНК [реал-тайм ПЦР]
Mycoplasma pneumoniae, ДНК [ПЦР]
Adenovirus, ДНК [реал-тайм ПЦР]
Streptococcus pneumoniae, ДНК [реал-тайм ПЦР]
Кто назначает исследование?
Инфекционист, терапевт, врач общей практики, педиатр, эпидемиолог.
Литература
Инфекционные болезни: национальное руководство / Под ред. Н. Д. Ющука, Ю. Я. Венгерова. — М.: ГЭОТАР-Медиа, 2009. С. 701-710.
Клиническая лабораторная диагностика: национальное руководство: в 2 т. — T. II / Под ред. В. В. Долгова, В. В. Меньшикова. — М.: ГЭОТАР-Медиа, 2012. С. 649-653.
Guidance for Clinicians on the Use of RT-PCR and Other Molecular Assays for Diagnosis of Influenza Virus Infection by Centers of Disease Control and Prevention, U.S. Department of Health and Human Services, 2016.
Henry’s Clinical Diagnosis and Management by Laboratory Methods, 23e by Richard A. McPherson MD MSc (), Matthew R. Pincus MD PhD (). St. Louis, Missouri : Elsevier, 2016. Page 1316.
- Debjit B., Rishab B., Darsh G., Parshuram R., Sampath K. P. K. Gastroretentive drug delivery systems- a novel approaches of control drug delivery systems. Research Journal of Science and Technology;10(2): 145–156. DOI: 10.5958/2349-2988.2018.00022.0.
- Мустафин Р. И., Протасова А. А., Буховец А. В., Семина И.И. Исследование интерполимерных сочетаний на основе (мет)акрилатов в качестве перспективных носителей в поликомплексных системах для гастроретентивной доставки. Фармация. 2014; 5: 3–5.
- Мирский, «Хирургия от древности до современности. Очерки истории.» (Москва, Наука, 2000, 798 с.).
- https://aptstore.ru/articles/gripp-a-chto-/.
- https://ru.qaz.wiki/wiki/Influenza_A_virus_subtype_H3N2.
- https://helix.ru/kb/item/09-171.
- Puccinotti, «Storia della medicina» (Ливорно, 1954—1959).
- Guardia, «La Médecine à travers les âges».
- А.В. Ланцова, Е.В. Санарова, Н.А. Оборотова и др. Разработка технологии получения инъекционной лекарственной формы на основе отечественной субстанции производной индолокарбазола ЛХС-1208 // Российский биотерапевтический журнал. 2014. Т. 13. № 3. С. 25-32.
- Wise, «Review of the History of Medicine» (Л., 1967).